诺希山:国家药物不良反应监督中心,迄今一共接到12份使用福尔可定后的17种不良反应报告。
卫生部指出,该部属下的药物管制局(PBKD)已在本月20日(周一)同意取消福尔可定(pholcodine)药物的注册,并指示召回所有含此成分的注册产品。
卫生总监丹斯里诺希山周四(23日)发文告说,这是基于存在已被发现的安全隐忧,也就是在全身麻醉过程中使用肌肉松弛药物或神经肌肉阻滞剂(NMBA),将发生过敏性休克风险,以及曾在过去12个月服用福尔可定药物的患者风险更高。
“换言之,曾在过去12个月服用福尔可定药物(通常是止咳药)的人士,若他们在全身麻醉过程中,如在手术时被施以肌肉松弛剂或神经肌肉阻滞剂 ,则面临更高的过敏性休克风险。”
他解释,药物管制局的上述决定是基于“对神经肌肉阻滞剂过敏和福尔可定暴露”(ALPHO)研究的证据、上市后的安全数据和医药人员提供的资料,并参考其他国家如英国、澳州,以及法国和挪威等欧盟国家,已采取监管行动取消注册和召回含福尔可定产品的做法。
诺希山说,福尔可定是一款用于减缓和停止成人和儿童干咳的药物,在大马,它被归类为C组管制药物,无需处方即可获取,以及一共有14款含福尔可定的产品,已向药物管制局注册。
他指出,截至目前,国家药剂监管局(NPRA)属下的国家药物不良反应监督中心,一共接到12份使用福尔可定后的17种不良反应报告,但这之中,没有过敏性休克的个案。
“福尔可定药物的注册在被取消后,所有的产品注册持有公司有责任通知早前已获得供应的社区药房和诊所,以停止销售,并确保产品在退回给供应商之前,隔离存放。”
“正在服用感冒咳嗽药的民众受促留意,以查看产品包装的标签或说明书是否含福尔可定活性成分。”
诺希山提到,如发现药物含福尔可定活性成分,应停止服用并咨询医药人员替代疗法,至于需接受手术并需要全身麻醉的人士,若曾服用含有福尔可定药物,尤其是在过去12个月,务必告知医药人员。
卫生部鼓励民众向国家药剂监管局通报任何的不良反应,可登录该局官网www.npra.gov.my,填写消费人副作用通报表(ConSERF)。
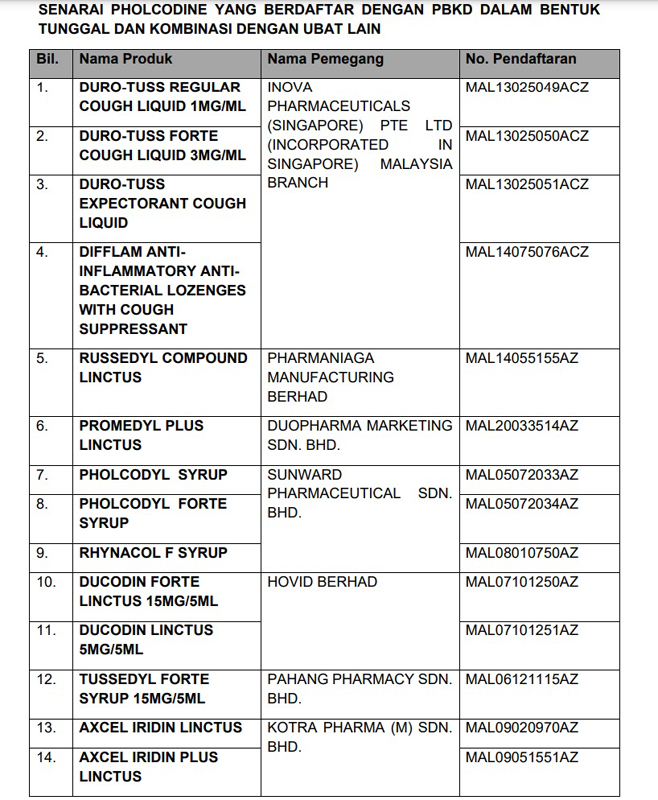
我国14款含福尔可定的注册产品如下:
1.DURO-TUSS REGULAR COUGH LIQUID 1MG/ML
2.DURO-TUSS FORTE COUGH LIQUID 3MG/ML
3.DURO-TUSS EXPECTORANT COUGH LIQUID
4.DIFFLAM ANTIINFLAMMATORY ANTIBACTERIAL LOZENGES WITH COUGH SUPPRESSANT
5.RUSSEDYL COMPOUND LINCTUS
6.PROMEDYL PLUS LINCTUS
7.PHOLCODYL SYRUP
8.PHOLCODYL FORTE SYRUP
9.RHYNACOL F SYRUP
10.DUCODIN FORTE LINCTUS 15MG/5ML
11.DUCODIN LINCTUS 5MG/5ML
12.TUSSEDYL FORTE SYRUP 15MG/5ML
13.AXCEL IRIDIN LINCTUS
14.AXCEL IRIDIN PLUS LINCTUS
来源:马新社